In ons tyd het fisika 'n baie algemene wetenskap geword. Dit is letterlik oral teenwoordig. Die mees elementêre voorbeeld: 'n appelboom groei in jou tuin, en vrugte word daarop ryp, die tyd kom en die appels begin val, maar in watter rigting val hulle? Danksy die wet van universele gravitasie val ons fetus op die grond, dit wil sê dit gaan af, maar nie op nie. Dit was een van die bekendste voorbeelde van fisika, maar kom ons gee aandag aan termodinamika, of meer presies, aan fase-ewewigte, wat nie minder belangrik is in ons lewe nie.
Termodinamika

Kom ons kyk eerstens na hierdie term. ΘερΜοδυναΜική - dit is hoe die woord in Grieks lyk. Die eerste deel ΘερΜo beteken "warmte", en die tweede δυναΜική beteken "krag". Termodinamika is 'n tak van fisika wat die eienskappe van 'n makroskopiese stelsel bestudeer, sowel as verskeie maniere om energie om te skakel en oor te dra. In hierdie afdeling word verskeie toestande en prosesse spesiaal bestudeer sodat die konsep van temperatuur in die beskrywing ingebring kan word (dit is 'n fisiese grootheid wat 'n termodinamiese sisteem kenmerk en gemeet word d.m.v.sekere toestelle). Alle deurlopende prosesse in termodinamiese stelsels word slegs beskryf deur mikroskopiese hoeveelhede (druk en temperatuur, sowel as die konsentrasie van komponente).
Clapeyron-Clausius-vergelyking
Elke fisikus ken hierdie vergelyking, maar kom ons breek dit stukkie vir stukkie af. Dit verwys na die ewewigsprosesse van die oorgang van sekere materie van een fase na 'n ander. Dit word duidelik gesien in sulke voorbeelde: smelt, verdamping, sublimasie (een van die maniere om produkte te bewaar, wat plaasvind deur vog heeltemal te verwyder). Die formule toon duidelik die deurlopende prosesse aan:
- n=PV/RT;
- waar T die temperatuur van die stof is;
- P-druk;
- R-spesifieke hitte van fase-oorgang;
- V-verandering in spesifieke volume.
Die geskiedenis van die skepping van die vergelyking

Die Clausius-Clapeyron-vergelyking is 'n uitstekende wiskundige verduideliking van die tweede wet van termodinamika. Ook na verwys as die "Clausius-ongelykheid". Die stelling is natuurlik ontwikkel deur die wetenskaplike self, wat die verband tussen die hittevloei in die sisteem en entropie, sowel as die omgewing daarvan, wou verduidelik. Hierdie vergelyking is deur Clausius ontwikkel in sy pogings om entropie te verklaar en te kwantifiseer. In die letterlike sin gee die stelling ons die geleentheid om te bepaal of 'n sikliese proses omkeerbaar of onomkeerbaar is. Hierdie ongelykheid bied vir ons 'n kwantitatiewe formule om die tweede wet te verstaan.
Die wetenskaplike was een van die eerstes wat aan die idee van entropie gewerk het, en het dit selfs gegeeproses naam. Wat nou bekend staan as Clausius se stelling is die eerste keer in 1862 gepubliseer in Rudolf se sesde werk, On the Use of the Transformation Equivalence Stelling for Interior Work. Die wetenskaplike het probeer om 'n proporsionele verband tussen entropie en energievloei deur verhitting (δ Q) in die stelsel aan te toon. In konstruksie kan hierdie termiese energie in werk omgeskakel word, en dit kan deur 'n sikliese proses in hitte omskep word. Rudolph het bewys dat "die algebraïese som van alle transformasies wat in 'n sikliese proses plaasvind, slegs minder as nul kan wees of, in uiterste gevalle, gelyk aan nul."
Geslote geïsoleerde stelsel
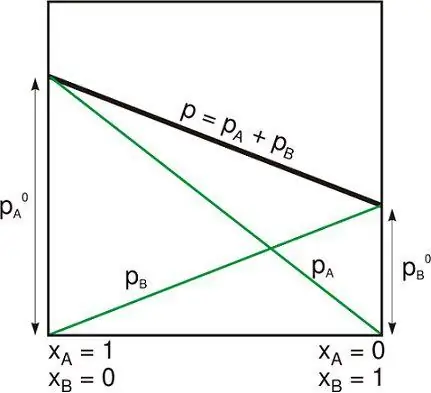
Geïsoleerde stelsel is een van die volgende:
- Fisiese stelsel is ver van ander wat nie met hulle interaksie het nie.
- Die termodinamiese stelsel word gesluit deur stewige onbeweegbare mure waardeur nie materie of energie kan beweeg nie.
Ondanks die feit dat die onderwerp intern verwant is aan sy eie swaartekrag, word 'n geïsoleerde sisteem gewoonlik verby die grense van eksterne gravitasie- en ander verafgeleë kragte geneem.
Dit kan gekontrasteer word met wat (in die meer algemene terminologie wat in termodinamika gebruik word) 'n geslote sisteem genoem word omring deur selektiewe mure waardeur energie in die vorm van hitte of werk oorgedra kan word, maar nie materie nie. En met 'n oop sisteem waarin materie en energie in- of uitgaan, hoewel dit verskeie ondeurdringbare mure indele van sy grense.
'n Geïsoleerde stelsel gehoorsaam die bewaringswet. In termodinamika word materie en energie meestal as aparte konsepte beskou.
Termodinamiese oorgange
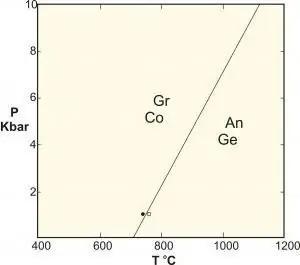
Om kwantumfase-oorgange te verstaan, is dit nuttig om dit met klassieke transformasies (ook genoem termiese inversies) te vergelyk. CPT beskryf die punt in die termodinamiese eienskappe van 'n sisteem. Dit dui op die herorganisasie van deeltjies. 'n Tipiese voorbeeld is die vriesende oorgang van water, wat 'n gladde oorgang tussen 'n vloeistof en 'n vaste stof beskryf. Klassieke fasegroei is te wyte aan die mededinging tussen die energie van die stelsel en die entropie van sy termiese skommelinge.
'n Klassieke stelsel het geen entropie by nultemperatuur nie en daarom kan geen fasetransformasie plaasvind nie. Hulle volgorde word bepaal deur die eerste diskontinue afgeleide termodinamiese potensiaal. En natuurlik het dit die eerste bestelling. Fasetransformasies van 'n ferromagneet na 'n paramagneet is kontinu en tweede orde. Hierdie konstante veranderinge van 'n geordende na 'n wanordelike fase word beskryf deur 'n ordeparameter wat nul is. Vir die bogenoemde ferromagnetiese transformasie sal die ordeparameter die totale magnetisering van die stelsel wees.
Gibbs-potensiaal
The Gibbs Free Energy is die maksimum hoeveelheid werk sonder uitbreiding wat verwyder kan word van 'n termodinamiese geslote stelsel (wat hitte kan uitruil en met die omgewing kan werk). Sulkedie maksimum resultaat kan slegs in 'n heeltemal omkeerbare proses verkry word. Wanneer die stelsel terugtransformeer van die eerste toestand na die tweede, is die vermindering in die Gibbs vrye energie gelyk aan dié wat deur die stelsel in sy omgewing uitgevoer word, minus die werk van die drukkragte.
State van balans

Termodinamiese en meganiese ewewig is 'n aksiomatiese konsep van termodinamika. Dit is die interne toestand van een of meer stelsels wat deur min of meer deurlaatbare of ondeurdringbare mure verbind is. In hierdie toestand is daar geen suiwer makroskopiese vloei van materie of energie nie, hetsy binne 'n sisteem of tussen sisteme.
In sy eie opvatting van die toestand van interne ewewig vind makroskopiese verandering nie plaas nie. Die stelsels is gelyktydig in wedersydse termiese, meganiese, chemiese (konstante), stralingsewewigte. Hulle kan in dieselfde vorm wees. In hierdie proses word alle aansigte gelyktydig en onbepaald gestoor totdat die fisiese bewerking verbreek word. In makroskopiese ewewig vind perfek presiese gebalanseerde uitruilings plaas. Bogenoemde bewys is 'n fisiese verduideliking van hierdie konsep.
Basies
Elke wette, stellings, formules het hul eie grondslae. Kom ons kyk na die 3 grondslae van die wet van fase-ewewig.
- Fase is 'n vorm van materie, homogeen in chemiese samestelling, fisiese toestand en meganiese balans. Tipiese fases is vaste, vloeistof en gasvormig. Twee onmengbare vloeistowwe (of vloeibare mengsels met verskillende samestellings) geskei deur 'n aparte grens word as twee afsonderlike fases en onmengbare vaste stowwe beskou.
- Die aantal komponente (C) is die aantal chemies onafhanklike komponente van die stelsel. Die minimum aantal onafhanklike spesies wat benodig word om die samestelling van alle fases van die stelsel te bepaal.
- Die aantal grade van vryheid (F) in hierdie konteks is die aantal intensiewe veranderlikes wat onafhanklik van mekaar is.
Klassifikasie volgens fase-ewewigte
- Reaksies van aaneenlopende netto oordrag (dikwels genoem vastestofreaksies) vind plaas tussen vaste stof van verskillende samestelling. Dit kan elemente insluit wat in vloeistowwe voorkom (H, C), maar hierdie elemente word in vaste fases behou, dus is geen vloeistoffases betrokke as reaktante of produkte nie (H2O, CO2). Soliede suiwer oordragreaksies kan kontinu of diskontinu, of terminaal wees.
- Polimorfies is 'n spesiale tipe vastefasereaksie wat fases van identiese samestelling insluit. Klassieke voorbeelde is die reaksies tussen aluminiumsilikate kianiet-sillimaniet-andalusiet, die omskakeling van grafiet na diamant by hoë druk, en die ewewig van kalsiumkarbonaat.
Wette van ewewig

The Gibbs Factory Rule is voorgestel deur Josiah Willard Gibbs in sy beroemde artikel getiteld "The Equilibrium of Heterogeneous Substances", wat van 1875 tot 1878 verskyn het. Dit is van toepassing opnie-reaktiewe multikomponent heterogene stelsels in termodinamiese ewewig en is 'n gegewe gelykheid:
- F=C-P+2;
- waar F die aantal grade van vryheid is;
- C - aantal komponente;
- P - aantal fases in termodinamiese ewewig met mekaar.
Die aantal grade van vryheid is die aantal onbesette intensiewe veranderlikes. Die grootste aantal termodinamiese parameters, soos temperatuur of druk, wat gelyktydig en arbitrêr kan wissel sonder om mekaar te beïnvloed. 'n Voorbeeld van 'n eenkomponentstelsel is een met 'n enkele suiwer chemikalie, terwyl tweekomponentstelsels, soos mengsels van water en etanol, twee onafhanklike komponente het. Tipiese fase-oorgange (fase-ewewig) is vaste stowwe, vloeistowwe, gasse.
Fasereël teen konstante druk
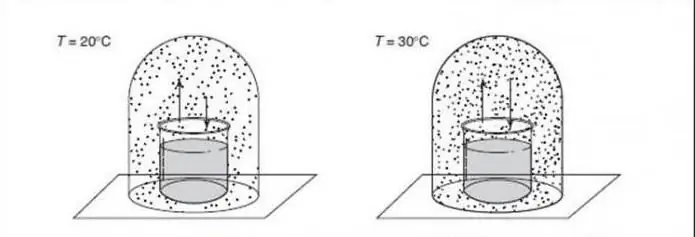
Vir toepassings in materiaalwetenskap wat handel oor faseveranderinge tussen verskillende vaste strukture, vind 'n konstante druk dikwels plaas (bv. een atmosfeer) en word geïgnoreer as 'n mate van vryheid, dus word die reël: F=C - P + 1.
Hierdie formule word soms ingestel onder die naam "gekondenseerde fase-reël", maar soos ons weet, is dit nie van toepassing op hierdie stelsels wat onderworpe is aan hoë druk (byvoorbeeld in geologie), aangesien die gevolge van hierdie druk kan katastrofiese gevolge veroorsaak.
Dit mag lyk asof fase-ewewig net 'n leë frase is, en daar is min fisiese prosesse waarin hierdie oomblikbetrokke is, maar, soos ons gesien het, daarsonder werk baie van die wette wat ons ken nie, so jy moet 'n bietjie vertroud raak met hierdie unieke, kleurvolle, al is dit 'n bietjie vervelige reëls. Hierdie kennis het baie mense gehelp. Hulle het geleer hoe om dit op hulself toe te pas, byvoorbeeld, elektrisiëns, met kennis van die reëls om met fases te werk, kan hulself teen onnodige gevaar beskerm.






