Termodinamika is 'n belangrike tak van fisika. Ons kan met sekerheid sê dat die prestasies daarvan gelei het tot die ontstaan van die tegnologiese era en grootliks die verloop van die menslike geskiedenis oor die afgelope 300 jaar bepaal het. Die artikel bespreek die eerste, tweede en derde wette van termodinamika en die toepassing daarvan in die praktyk.
Wat is termodinamika?
Voordat ons die wette van termodinamika formuleer, laat ons uitvind wat hierdie afdeling van fisika doen.
Die woord "termodinamika" is van Griekse oorsprong en beteken "beweging as gevolg van hitte". Dit wil sê, hierdie tak van fisika is besig met die bestudering van enige prosesse, as gevolg waarvan termiese energie omgeskakel word in meganiese beweging en omgekeerd.
Die basiese wette van termodinamika is in die middel van die 19de eeu geformuleer. Die wetenskap van "beweging en hitte" beskou die gedrag van die hele stelsel as 'n geheel, bestudeer die verandering in sy makroskopiese parameters - temperatuur, druk en volume, en gee nie aandag aan sy mikroskopiese struktuur nie. Boonop speel die eerste daarvan 'n fundamentele rol in die formulering van wettetermodinamika in fisika. Dit is eienaardig om daarop te let dat hulle uitsluitlik van eksperimentele waarnemings afgelei is.
Die konsep van 'n termodinamiese stelsel

Dit beteken enige groep atome, molekules of ander elemente wat as 'n geheel beskou word. Al drie wette is geformuleer vir die sogenaamde termodinamiese sisteem. Voorbeelde is: die Aarde se atmosfeer, enige lewende organisme, die gasmengsel in 'n binnebrandenjin, ens.
Alle stelsels in termodinamika behoort aan een van drie tipes:
- Oop. Hulle ruil beide hitte en materie met die omgewing uit. As kos byvoorbeeld in 'n pot op 'n oop vuur gekook word, is dit 'n aanskoulike voorbeeld van 'n oop sisteem, aangesien die pot energie van die eksterne omgewing (vuur) ontvang, terwyl dit self energie in die vorm van hitte uitstraal, en water verdamp ook daaruit (metabolisme)
- Geslote. In sulke stelsels is daar geen uitruiling van materie met die omgewing nie, alhoewel die uitruiling van energie plaasvind. Om terug te keer na die vorige geval: as jy die ketel met 'n deksel bedek, kan jy 'n geslote stelsel kry.
- Geïsoleerd. Dit is 'n soort termodinamiese stelsels wat nie materie of energie met die omliggende ruimte uitruil nie. 'n Voorbeeld sou 'n termosfles wees wat warm tee bevat.
Termodinamiese temperatuur

Hierdie konsep beteken die kinetiese energie van die deeltjies wat die omliggende liggame vorm, wat die spoed weerspieëlewekansige beweging van deeltjies. Hoe groter dit is, hoe hoër is die temperatuur. Gevolglik, deur die kinetiese energie van die stelsel te verminder, verkoel ons dit.
Hierdie konsep beteken die kinetiese energie van die deeltjies wat die omliggende liggame vorm, wat die spoed van die chaotiese beweging van deeltjies weerspieël. Hoe groter dit is, hoe hoër is die temperatuur. Gevolglik, deur die kinetiese energie van die stelsel te verminder, verkoel ons dit.
Termodinamiese temperatuur word uitgedruk in SI (International System of Units) in Kelvin (ter ere van die Britse wetenskaplike William Kelvin, wat hierdie skaal eerste voorgestel het). Om die eerste, tweede en derde wette van termodinamika te verstaan is onmoontlik sonder 'n definisie van temperatuur.
'n Deling van een graad op die Kelvin-skaal stem ook ooreen met een graad Celsius. Die omskakeling tussen hierdie eenhede word uitgevoer volgens die formule: TK =TC + 273, 15, waar TK en TC - temperature in onderskeidelik kelvine en grade Celsius.
Die eienaardigheid van die Kelvin-skaal is dat dit nie negatiewe waardes het nie. Nul daarin (TC=-273, 15 oC) stem ooreen met die toestand wanneer die termiese beweging van die deeltjies van die stelsel heeltemal afwesig is, dit lyk asof hulle "gevries" is.
Bewaring van energie en die 1ste wet van termodinamika

In 1824 het Nicolas Léonard Sadi Carnot, 'n Franse ingenieur en fisikus, 'n dapper voorstel gemaak wat nie net tot die ontwikkeling van fisika gelei het nie, maar ook 'n groot stap in die verbetering van tegnologie geword het. Synekan soos volg geformuleer word: "Energie kan nie geskep of vernietig word nie, dit kan slegs van een staat na 'n ander oorgedra word."
Trouens, Sadi Carnot se frase postuleer die wet van behoud van energie, wat die basis van die 1ste wet van termodinamika gevorm het: "Wanneer 'n sisteem energie van buite ontvang, skakel dit dit om in ander vorme, die hoof van wat termies en meganies is."
Die wiskundige formule vir die 1ste wet is soos volg geskryf:
Q=ΔU + A, hier Q is die hoeveelheid hitte wat deur die omgewing na die stelsel oorgedra word, ΔU is die verandering in die interne energie van hierdie stelsel, A is die perfekte meganiese werk.
Adiabatiese prosesse
'n Goeie voorbeeld daarvan is die beweging van lugmassas langs berghange. Sulke massas is groot (kilometer of meer), en lug is 'n uitstekende hitte-isolator. Die genoteerde eienskappe stel ons in staat om enige prosesse met lugmassas wat binne 'n kort tyd plaasvind as adiabaties te beskou. Wanneer lug teen 'n berghelling opstyg, daal die druk, dit brei uit, dit wil sê, dit verrig meganiese werk, en as gevolg daarvan koel dit af. Inteendeel, die afwaartse beweging van die lugmassa gaan gepaard met 'n toename in druk daarin, dit druk saam en word as gevolg hiervan baie warm.
Die toepassing van die wet van termodinamika, wat in die vorige subopskrif bespreek is, word die maklikste gedemonstreer deur die voorbeeld van 'n adiabatiese proses te gebruik.
Volgens die definisie is daar as gevolg daarvan geen uitruil van energie metomgewing, dit wil sê in die vergelyking hierbo, Q=0. Dit lei tot die volgende uitdrukking: ΔU=-A. Die minus teken hier beteken dat die stelsel meganiese werk verrig deur sy eie interne energie te verminder. Daar moet onthou word dat die interne energie direk afhanklik is van die temperatuur van die stelsel.
Richting van termiese prosesse
Hierdie uitgawe handel oor die 2de wet van termodinamika. Almal het sekerlik opgemerk dat as jy twee voorwerpe met verskillende temperature in aanraking bring, dan sal die koue een altyd warm word, en die warm een sal afkoel. Let daarop dat die omgekeerde proses binne die raamwerk van die eerste wet van termodinamika kan plaasvind, maar dit word nooit in die praktyk geïmplementeer nie.
Die rede vir die onomkeerbaarheid van hierdie proses (en alle bekende prosesse in die Heelal) is die oorgang van die stelsel na 'n meer waarskynlike toestand. In die beskoude voorbeeld met die kontak van twee liggame van verskillende temperature, sal die mees waarskynlike toestand die een wees waarin alle deeltjies van die sisteem dieselfde kinetiese energie sal hê.
Die tweede wet van termodinamika kan soos volg geformuleer word: "Hitte kan nooit spontaan van 'n koue liggaam na 'n warm een oorgedra word nie." As ons die konsep van entropie as 'n maatstaf van wanorde bekendstel, dan kan dit soos volg voorgestel word: "Enige termodinamiese proses gaan voort met 'n toename in entropie".
Hitte-enjin

Hierdie term word verstaan as 'n stelsel wat, as gevolg van die toevoer van eksterne energie daaraan, meganiese werk kan verrig. Eerstenshitte-enjins was stoomenjins en is aan die einde van die 17de eeu uitgevind.
Die tweede wet van termodinamika speel 'n deurslaggewende rol in die bepaling van hul doeltreffendheid. Sadi Carnot het ook vasgestel dat die maksimum doeltreffendheid van hierdie toestel is: Doeltreffendheid=(T2 - T1)/T2, hier is T2 en T1 verwarmer- en yskastemperature. Meganiese werk kan slegs gedoen word wanneer daar 'n hittevloei van 'n warm liggaam na 'n koue een is, en hierdie vloei kan nie 100% in nuttige energie omgeskakel word nie.
Die figuur hieronder toon die werkingsbeginsel van 'n hitte-enjin (Qabs - hitte oorgedra na die masjien, Qced - hitteverlies, W - nuttige werk, P en V - druk en volume gas in die suier).
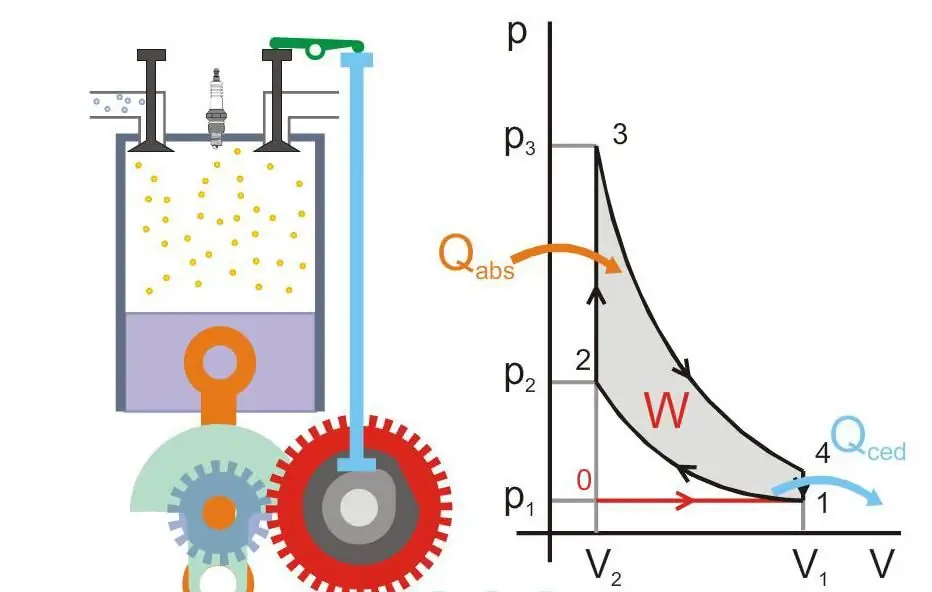
Absolute nul en Nernst se postulaat
Laastens, kom ons gaan oor na die oorweging van die derde wet van termodinamika. Dit word ook die Nernst-postulaat genoem (die naam van die Duitse fisikus wat dit die eerste keer aan die begin van die 20ste eeu geformuleer het). Die wet sê: "Absolute nul kan nie bereik word met 'n eindige aantal prosesse nie." Dit wil sê, dit is op enige manier onmoontlik om die molekules en atome van 'n stof heeltemal te "vries". Die rede hiervoor is die konstante bestaande hitte-uitruiling met die omgewing.

Een nuttige gevolgtrekking wat uit die derde wet van termodinamika gemaak word, is dat entropie afneem soos mens na absolute nul beweeg. Dit beteken dat die stelsel geneig is om homself te organiseer. Hierdie feit kangebruik byvoorbeeld om paramagnete na 'n ferromagnetiese toestand oor te dra wanneer dit afgekoel word.
Dit is interessant om daarop te let dat die laagste temperatuur wat tot dusver bereik is 5·10−10 K (2003, MIT-laboratorium, VSA).






