Ideale gas, die ideale gasvergelyking van toestand, sy temperatuur en druk, volume… die lys parameters en definisies wat in die ooreenstemmende afdeling van fisika gebruik word, kan nogal lank voortgesit word. Vandag sal ons net oor hierdie onderwerp praat.
Wat word in molekulêre fisika oorweeg?

Die hoofvoorwerp wat in hierdie afdeling oorweeg word, is 'n ideale gas. Die ideale gasvergelyking van toestand is verkry met inagneming van normale omgewingstoestande, en ons sal 'n bietjie later hieroor praat. Kom ons benader hierdie "probleem" nou van ver af.
Kom ons sê ons het 'n mate van gas. Die toestand daarvan kan bepaal word deur drie parameters van 'n termodinamiese aard te gebruik. Dit is natuurlik druk, volume en temperatuur. Die vergelyking van die toestand van die stelsel in hierdie geval sal die formule wees vir die verband tussen die ooreenstemmende parameters. Dit lyk so: F (p, V, T)=0.
Hier, vir die eerste keer, nader ons stadigaan die ontstaan van so iets soos ideaalgas. Dit word 'n gas genoem waarin die interaksies tussen molekules weglaatbaar is. Oor die algemeen bestaan dit nie in die natuur nie. Enige hoogs verskeurde gas is egter naby daaraan. Stikstof, suurstof en lug, wat onder normale toestande is, verskil min van die ideaal. Om die toestandsvergelyking vir 'n ideale gas te skryf, kan ons die verenigde gaswet gebruik. Ons kry: pV/T=konst.
Verwante konsep 1: Avogadro se wet
Hy kan vir ons sê dat as ons dieselfde aantal mol van absoluut enige willekeurige gas neem en dit in dieselfde toestande plaas, insluitend temperatuur en druk, dan sal die gasse dieselfde volume beset. Die eksperiment is veral onder normale toestande uitgevoer. Dit beteken dat die temperatuur 273,15 Kelvin was, die druk was een atmosfeer (760 millimeter kwik, of 101325 Pascal). Met hierdie parameters het die gas 'n volume gelykstaande aan 22,4 liter beset. Daarom kan ons sê dat vir een mol van enige gas die verhouding van numeriese parameters 'n konstante waarde sal wees. Daarom is besluit om hierdie figuur met die letter R aan te dui en dit die universele gaskonstante te noem. Dit is dus gelyk aan 8,31. Die eenheid is J/molK.
Ideale gas. Die ideale gasvergelyking van toestand en sy manipulasie
Kom ons probeer om die formule te herskryf. Om dit te doen, skryf ons dit in hierdie vorm: pV=RT. Vervolgens voer ons 'n eenvoudige aksie uit, vermenigvuldig beide kante van die vergelyking met 'n arbitrêre aantal mol. Ons kry pVu=uRT. Kom ons neem die feit in ag dat die produk van die molêre volume endie hoeveelheid materie is bloot die volume. Maar die aantal mol sal tog gelyktydig gelyk wees aan die kwosiënt van die massa en die molêre massa. Dit is presies hoe die Mendeleev-Clapeyron-vergelyking lyk. Dit gee 'n duidelike idee van watter soort stelsel 'n ideale gas vorm. Die toestandsvergelyking vir 'n ideale gas sal die vorm aanneem: pV=mRT/M.
Lei die formule vir druk af
Kom ons doen nog 'n paar manipulasies met die verkrygde uitdrukkings. Om dit te doen, word die regterkant van die Mendeleev-Clapeyron-vergelyking vermenigvuldig en gedeel deur die Avogadro-getal. Nou kyk ons noukeurig na die produk van die hoeveelheid stof deur die Avogadro-getal. Dit is niks anders as die totale aantal molekules in die gas nie. Maar terselfdertyd sal die verhouding van die universele gaskonstante tot die Avogadro-getal gelyk wees aan die Boltzmann-konstante. Daarom kan formules vir druk soos volg geskryf word: p=NkT/V of p=nkT. Hier is die simbool n die deeltjiekonsentrasie.
Ideale gasprosesse
In molekulêre fisika is daar iets soos isoprosesse. Dit is termodinamiese prosesse wat in die sisteem by een van die konstante parameters plaasvind. In hierdie geval moet die massa van die stof ook konstant bly. Kom ons kyk meer spesifiek na hulle. Dus, die wette van 'n ideale gas.
Druk bly konstant
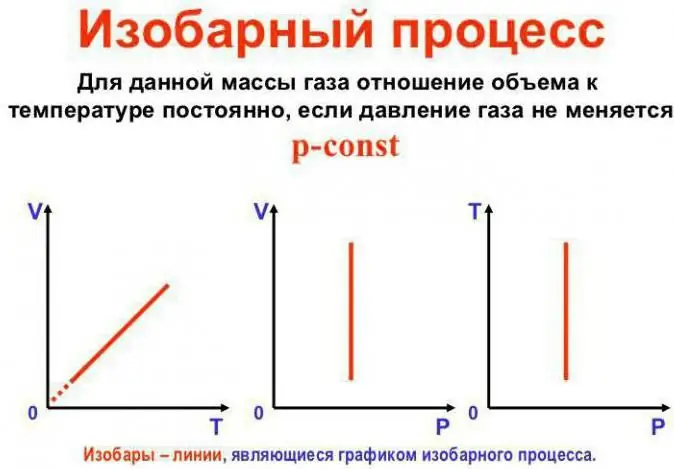
Dit is Gay-Lussac se wet. Dit lyk so: V/T=konst. Dit kan op 'n ander manier herskryf word: V=Vo (1 + at). Hier is a gelyk aan 1/273.15 K^-1 en word die "volume-uitbreidingskoëffisiënt" genoem. Ons kan die temperatuur vervang in beide Celsius endie Kelvin-skaal. In laasgenoemde geval kry ons die formule V=Voat.
Volume bly konstant

Dit is Gay-Lussac se tweede wet, meer algemeen na verwys as Charles se wet. Dit lyk so: p/T=konst. Daar is nog 'n formulering: p=po (1 + at). Transformasies kan volgens die vorige voorbeeld uitgevoer word. Soos jy kan sien, is die ideale gaswette soms baie soortgelyk aan mekaar.
Temperatuur bly konstant

As die temperatuur van 'n ideale gas konstant bly, dan kan ons die Boyle-Mariotte-wet kry. Dit kan so geskryf word: pV=const.
Verwante konsep 2: gedeeltelike druk
Kom ons sê ons het 'n vaartuig met gasse. Dit sal 'n mengsel wees. Die stelsel is in 'n toestand van termiese ewewig, en die gasse self reageer nie met mekaar nie. Hier sal N die totale aantal molekules aandui. N1, N2 ensovoorts, onderskeidelik, die aantal molekules in elk van die komponente van die mengsel. Kom ons neem die drukformule p=nkT=NkT/V. Dit kan oopgemaak word vir 'n spesifieke geval. Vir 'n twee-komponent mengsel sal die formule die vorm aanneem: p=(N1 + N2) kT/V. Maar dan blyk dit dat die totale druk opgetel sal word uit die parsiële drukke van elke mengsel. So, dit sal lyk soos p1 + p2 en so aan. Dit sal die gedeeltelike druk wees.
Waarvoor is dit?
Die formule wat ons verkry het, dui aan dat die druk in die sisteem van elke groep molekules is. Terloops, dit hang nie af nieander. D alton het hiervan gebruik gemaak by die formulering van die wet, wat later na hom genoem is: in 'n mengsel waar gasse nie chemies met mekaar reageer nie, sal die totale druk gelyk wees aan die som van die parsiële drukke.






