Die hittekapasiteit van 'n gas is die hoeveelheid energie wat 'n liggaam absorbeer wanneer dit met een graad verhit word. Kom ons ontleed die hoofkenmerke van hierdie fisiese hoeveelheid.

Definisies
Die spesifieke hitte van 'n gas is die eenheidsmassa van 'n bepaalde stof. Sy maateenhede is J/(kg·K). Die hoeveelheid hitte wat deur die liggaam geabsorbeer word in die proses om sy toestand van aggregasie te verander, word nie net geassosieer met die aanvanklike en finale toestand nie, maar ook met die metode van oorgang.

Departement
Die hittekapasiteit van gasse word gedeel deur die waarde bepaal by konstante volume (Cv), konstante druk (Cр).
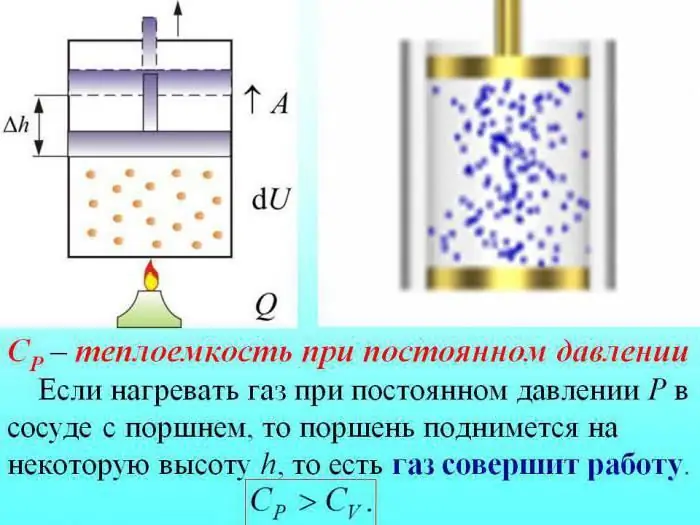
In die geval van verhitting sonder om die druk te verander, word 'n bietjie hitte bestee om die werk van gasuitsetting te produseer, en 'n deel van die energie word bestee om interne energie te verhoog.
Die hittekapasiteit van gasse by konstante druk word bepaal deur die hoeveelheid hitte wat spandeer word om interne energie te verhoog.
Gastoestand: kenmerke, beskrywing
Die hittekapasiteit van 'n ideale gas word bepaal met inagneming van die feit dat Сp-Сv=R. Laasgenoemde hoeveelheid word die universele gaskonstante genoem. Die waarde daarvan stem ooreen met 8,314 J/(mol K).
Wanneer teoretiese berekeninge van hittekapasiteit uitgevoer word, byvoorbeeld, om die verband met temperatuur te beskryf, is dit nie genoeg om slegs termodinamiese metodes te gebruik nie, dit is belangrik om jouself te bewapen met elemente van statiese fisika.
Die hittekapasiteit van gasse behels die berekening van die gemiddelde waarde van die energie van die translasiebeweging van sommige molekules. Sodanige beweging word saamgevat uit die rotasie- en translasiebeweging van die molekule, sowel as uit die interne vibrasies van atome.
In statiese fisika is daar inligting dat daar vir elke graad van vryheid van rotasie- en translasiebeweging 'n hoeveelheid vir 'n gas is wat gelyk is aan die helfte van die universele gaskonstante.

Interessante feite
Daar word aanvaar dat 'n deeltjie van 'n monoatomiese gas drie translasiegrade van vryheid het, dus het die spesifieke hitte van 'n gas drie translasie-, twee rotasie- en een vibrasievryheidsgrade. Die wet van hul eenvormige verspreiding lei daartoe dat die spesifieke hitte by 'n konstante volume gelykgestel word aan R.
Tydens die eksperimente is gevind dat die hittekapasiteit van 'n diatomiese gas ooreenstem met die waarde R. So 'n verskil tussen teorie en praktyk word verklaar deur die feit dat die hittekapasiteit van 'n ideale gas met kwantum geassosieer word gevolge, dus, wanneer berekeninge gemaak word, is dit belangrik om statistiek gebaseer op kwantum te gebruikmeganika.
Gebaseer op die fondamente van kwantummeganika, het enige stelsel van deeltjies wat ossilleer of roteer, insluitend gasmolekules, slegs 'n paar diskrete waardes van energie.
As die energie van termiese beweging in die stelsel nie genoeg is om ossillasies van 'n sekere frekwensie op te wek nie, dra sulke bewegings nie by tot die totale hittekapasiteit van die stelsel nie.
Gevolglik word 'n spesifieke mate van vryheid "gevries", dit is onmoontlik om die wet van gelykverdeling daarop toe te pas.
Die hittekapasiteit van gasse is 'n belangrike eienskap van die toestand waarvan die werking van die hele termodinamiese stelsel afhang.
Die temperatuur waarteen die wet van ekwipartisie toegepas kan word op die vibrasie- of rotasiegraad van vryheid word gekenmerk deur kwantumteorie, verbind die Planck-konstante met die Boltzmann-konstante.

Diatomiese gasse
Die gapings tussen die rotasie-energievlakke van sulke gasse is 'n klein aantal grade. Die uitsondering is waterstof, waarin die temperatuurwaarde deur honderde grade bepaal word.
Daarom is die hittekapasiteit van 'n gas by konstante druk moeilik om te beskryf deur die wet van eenvormige verspreiding. In kwantumstatistieke word by die bepaling van die hittekapasiteit in ag geneem dat sy vibrasiedeel, in die geval van 'n afname in temperatuur, vinnig afneem en nul bereik.
Hierdie verskynsel verklaar die feit dat daar by kamertemperatuur feitlik geen vibrasiedeel van die hittekapasiteit is nie, wantdiatomiese gas, dit stem ooreen met die konstante R.
Die hittekapasiteit van 'n gas by konstante volume in die geval van lae-temperatuur-aanwysers word bepaal met behulp van kwantumstatistieke. Daar is die Nernst-beginsel, wat die derde wet van termodinamika genoem word. Op grond van sy formulering sal die molêre hittekapasiteit van 'n gas afneem met dalende temperatuur, en neig na nul.

Kenmerke van vaste stowwe
As die hittekapasiteit van 'n mengsel van gasse verduidelik kan word deur gebruik te maak van kwantumstatistiek, dan word termiese beweging vir 'n vaste toestand van aggregasie gekenmerk deur geringe fluktuasies van deeltjies naby die ewewigsposisie.
Elke atoom het drie vibrasiegrade van vryheid, daarom kan, in ooreenstemming met die ekwipartisiewet, die molêre hittekapasiteit van 'n vaste stof as 3nR bereken word, met n die aantal atome in 'n molekule.
In praktyk is hierdie getal die limiet waartoe die hittekapasiteit van 'n soliede liggaam by hoë temperature neig.
Maksimum kan verkry word by gewone temperature vir sommige elemente, insluitend metale. Vir n=1 is die Dulong- en Petit-wet vervul, maar vir komplekse stowwe is dit nogal moeilik om so 'n limiet te bereik. Aangesien die limiet nie in werklikheid verkry kan word nie, vind ontbinding of smelting van die vaste stof plaas.
Geskiedenis van kwantumteorie
Die stigters van die kwantumteorie is Einstein en Debye aan die begin van die twintigste eeu. Dit is gebaseer op die kwantisering van ossillerende bewegings van atome in 'n sekerekristal. In die geval van lae temperatuur-aanwysers blyk die hittekapasiteit van 'n soliede liggaam direk eweredig te wees aan die absolute waarde wat in blokkies geneem word. Hierdie verhouding is Debye se wet genoem. As 'n maatstaf wat dit moontlik maak om tussen lae en hoë temperatuur aanwysers te onderskei, word hul vergelyking met die Debye temperatuur geneem.
Hierdie waarde word bepaal deur die spektrum van vibrasies van 'n atoom in die liggaam, daarom hang dit ernstig af van die kenmerke van sy kristalstruktuur.
QD is 'n waarde wat etlike honderde K het, maar dit is byvoorbeeld baie hoër in diamant.
Die geleidingselektrone lewer 'n beduidende bydrae tot die hittekapasiteit van metale. Om dit te bereken, word die Fermi-kwantumstatistieke gebruik. Die elektroniese geleidingsvermoë vir metaalatome is direk eweredig aan die absolute temperatuur. Aangesien dit 'n onbeduidende waarde is, word dit slegs in ag geneem by temperature wat na absolute nul neig.
Metodes vir die bepaling van hittekapasiteit
Die belangrikste eksperimentele metode is kalorimetrie. Om 'n teoretiese berekening van hittekapasiteit uit te voer, word statistiese termodinamika gebruik. Dit is geldig vir 'n ideale gas, sowel as vir kristallyne liggame, word uitgevoer op grond van eksperimentele data oor die struktuur van materie.
Empiriese metodes vir die berekening van die hittekapasiteit van 'n ideale gas is gebaseer op die idee van die chemiese struktuur, die bydrae van individuele groepe atome tot Ср.
Vir vloeistowwe word metodes ook gebruik wat gebaseer is op die gebruik van termodinamikasiklusse wat dit moontlik maak om van die hittekapasiteit van 'n ideale gas na 'n vloeistof oor te gaan deur die afgeleide van die temperatuur van die entalpie van die verdampingsproses.
In die geval van 'n oplossing word die berekening van die hittekapasiteit as 'n byvoegingsfunksie nie toegelaat nie, aangesien die oormaatwaarde van die hittekapasiteit van die oplossing basies betekenisvol is.
Om dit te evalueer, het ons die molekulêr-statistiese teorie van oplossings nodig. Die moeilikste is die identifisering van die hittekapasiteit van heterogene sisteme in termodinamiese analise.

Gevolgtrekking
Die studie van hittekapasiteit stel jou in staat om die energiebalans van prosesse wat in chemiese reaktore voorkom, sowel as in ander chemiese produksie-apparate te bereken. Boonop is hierdie waarde nodig vir die keuse van optimale tipes koelmiddels.
Op die oomblik is die eksperimentele bepaling van die hittekapasiteit van stowwe vir verskeie temperatuurintervalle - van lae waardes tot hoë waardes - die hoofopsie om die termodinamiese eienskappe van 'n stof te bepaal. Wanneer die entropie en entalpie van 'n stof bereken word, word hittekapasiteit-integrale gebruik. Inligting oor die hittekapasiteit van chemiese reagense in 'n sekere temperatuurreeks laat jou toe om die termiese effek van die proses te bereken. Inligting oor die hittekapasiteit van oplossings maak dit moontlik om hul termodinamiese parameters teen enige temperatuurwaardes binne die geanaliseerde interval te bereken.
Byvoorbeeld, 'n vloeistof word gekenmerk deur die besteding van 'n deel van die hitte om die waarde van potensiële energie te veranderreagerende molekules. Hierdie waarde word die "konfigurasie" hittekapasiteit genoem, wat gebruik word om oplossings te beskryf.
Dit is moeilik om volwaardige wiskundige berekeninge uit te voer sonder om die termodinamiese eienskappe van 'n stof, die toestand van aggregasie, in ag te neem. Daarom word vir vloeistowwe, gasse, vaste stowwe so 'n eienskap soos spesifieke hittekapasiteit gebruik, wat dit moontlik maak om die energieparameters van 'n stof te karakteriseer.






