Wanneer die gedrag van gasse in fisika bestudeer word, word baie aandag aan isoprosesse gegee, dit wil sê sulke oorgange tussen die toestande van die sisteem, waartydens een termodinamiese parameter behoue bly. Daar is egter 'n gasoorgang tussen state, wat nie 'n isoproses is nie, maar wat 'n belangrike rol in die natuur en tegnologie speel. Dit is 'n adiabatiese proses. In hierdie artikel sal ons dit in meer besonderhede oorweeg, met die fokus op wat die gas adiabatiese eksponent is.
Adiabatiese proses
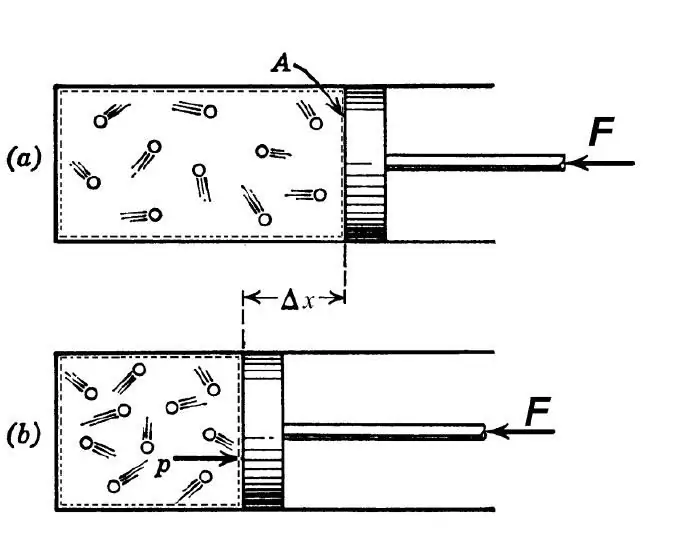
Volgens die termodinamiese definisie word 'n adiabatiese proses verstaan as so 'n oorgang tussen die aanvanklike en finale toestande van die sisteem, as gevolg waarvan daar geen hitte-uitruiling tussen die eksterne omgewing en die sisteem wat bestudeer word, plaasvind nie. So 'n proses is moontlik onder die volgende twee voorwaardes:
- termiese geleiding tussen die eksterne omgewing enstelsel is laag vir een of ander rede;
- die spoed van die proses is hoog, so die hitte-uitruiling het nie tyd om te plaasvind nie.
In ingenieurswese word die adiabatiese oorgang gebruik om die gas te verhit tydens sy skerp samedrukking en om dit af te koel tydens vinnige uitsetting. In die natuur manifesteer die betrokke termodinamiese oorgang hom wanneer 'n lugmassa teen 'n heuwel styg of daal. Sulke op- en afdraandes lei tot 'n verandering in die doupunt in die lug en neerslag.
Poisson se vergelyking vir die adiabatiese ideale gas

'n Ideale gas is 'n stelsel waarin deeltjies willekeurig teen hoë spoed beweeg, nie met mekaar in wisselwerking is nie en dimensieloos is. So 'n model is baie eenvoudig in terme van sy wiskundige beskrywing.
Volgens die definisie van 'n adiabatiese proses kan die volgende uitdrukking in ooreenstemming met die eerste wet van termodinamika geskryf word:
dU=-PdV.
Met ander woorde, 'n gas, wat uitbrei of saamtrek, werk wel PdV as gevolg van 'n ooreenstemmende verandering in sy interne energie dU.
In die geval van 'n ideale gas, as ons die toestandsvergelyking (Clapeyron-Mendeleev-wet) gebruik, kan ons die volgende uitdrukking kry:
PVγ=konst.
Hierdie gelykheid word die Poisson-vergelyking genoem. Mense wat vertroud is met gasfisika sal opmerk dat as die waarde van γ gelyk is aan 1, die Poisson-vergelyking in die Boyle-Mariotte-wet (isotermieseproses). So 'n transformasie van die vergelykings is egter onmoontlik, aangesien γ vir enige tipe ideale gas groter as een is. Die hoeveelheid γ (gamma) word die adiabatiese indeks van 'n ideale gas genoem. Kom ons kyk van nader na die fisiese betekenis daarvan.
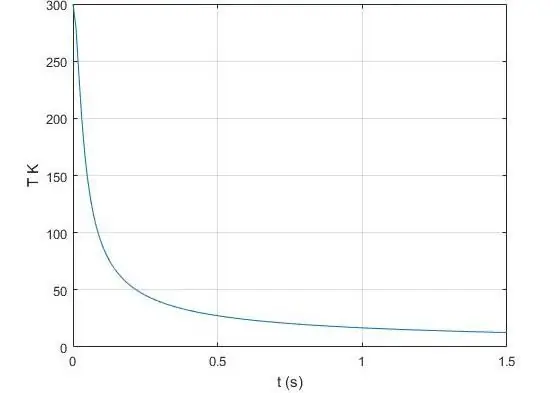
Wat is die adiabatiese eksponent?
Die eksponent γ, wat in die Poisson-vergelyking vir 'n ideale gas voorkom, is die verhouding van hittekapasiteit by konstante druk tot dieselfde waarde, maar reeds by konstante volume. In fisika is hittekapasiteit die hoeveelheid hitte wat na of geneem moet word van 'n gegewe sisteem sodat dit sy temperatuur met 1 Kelvin kan verander. Ons sal die isobariese hittekapasiteit aandui deur die simbool CP, en die isochoriese hittekapasiteit met die simbool CV. Dan geld die gelykheid vir γ:
γ=CP/CV.
Aangesien γ altyd groter as een is, wys dit hoeveel keer die isobariese hittekapasiteit van die bestudeerde gasstelsel die soortgelyke isochoriese eienskap oorskry.
Verhittingskapasiteite van CP en CV
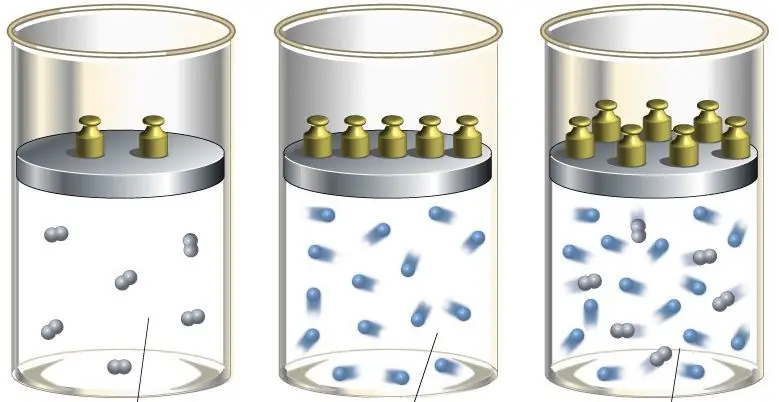
Om die adiabatiese eksponent te bepaal, moet 'n mens 'n goeie begrip hê van die betekenis van die hoeveelhede CP en CV. Om dit te doen, sal ons die volgende gedagte-eksperiment uitvoer: stel jou voor dat die gas in 'n geslote sisteem in 'n houer met soliede wande is. As die houer verhit word, sal al die gekommunikeerde hitte ideaal omgeskakel word in die interne energie van die gas. In so 'n situasie sal gelykheid geldig wees:
dU=CVdT.
WaardeCV definieer die hoeveelheid hitte wat na die stelsel oorgedra moet word om dit isochories met 1 K te verhit.
Sê nou die gas is in 'n vaartuig met 'n bewegende suier. In die proses om so 'n stelsel te verhit, sal die suier beweeg, wat verseker dat 'n konstante druk gehandhaaf word. Aangesien die entalpie van die sisteem in hierdie geval gelyk sal wees aan die produk van die isobariese hittekapasiteit en die verandering in temperatuur, sal die eerste wet van termodinamika die vorm aanneem:
CPdT=CVdT + PdV.
Van hier af kan gesien word dat CP>CV, aangesien dit in die geval van 'n isobariese verandering van toestande nodig is om spandeer hitte nie net om die temperatuur van die stelsel te verhoog nie, en dus sy interne energie, maar ook die werk wat deur die gas verrig word tydens sy uitbreiding.
Die waarde van γ vir 'n ideale monoatomiese gas
Die eenvoudigste gasstelsel is 'n monatomiese ideale gas. Gestel ons het 1 mol van so 'n gas. Onthou dat in die proses van isobariese verhitting van 1 mol gas met slegs 1 Kelvin, dit wel gelyk aan R werk. Hierdie simbool word algemeen gebruik om die universele gaskonstante aan te dui. Dit is gelyk aan 8, 314 J / (molK). Deur die laaste uitdrukking in die vorige paragraaf vir hierdie geval toe te pas, kry ons die volgende gelykheid:
CP=CV+ R.
Vanwaar jy die waarde van isochoriese hittekapasiteit kan bepaal CV:
γ=CP/CV;
CV=R/(γ-1).
Dit is bekend dat vir een moesiemonatomiese gas, die waarde van die isochoriese hittekapasiteit is:
CV=3/2R.
Van die laaste twee gelykhede volg die waarde van die adiabatiese eksponent:
3/2R=R/(γ-1)=>
γ=5/3 ≈ 1, 67.
Let daarop dat die waarde van γ uitsluitlik afhang van die interne eienskappe van die gas self (van die poliatomiese aard van sy molekules) en nie afhang van die hoeveelheid stof in die sisteem nie.
Afhanklikheid van γ van die aantal grade van vryheid
Die vergelyking vir die isochoriese hittekapasiteit van 'n monatomiese gas is hierbo geskryf. Die koëffisiënt 3/2 wat daarin verskyn het, hou verband met die aantal vryheidsgrade in een atoom. Dit het die vermoë om slegs in een van die drie rigtings van die ruimte te beweeg, dit wil sê, daar is slegs translasiegrade van vryheid.
As die sisteem deur diatomiese molekules gevorm word, word nog twee rotasiegrade by die drie translasiegrade gevoeg. Daarom word die uitdrukking vir CV:
CV=5/2R.
Dan sal die waarde van γ wees:
γ=7/5=1, 4.
Let daarop dat die diatomiese molekule eintlik nog een vibrasiegraad van vryheid het, maar by temperature van etlike honderde Kelvin word dit nie geaktiveer nie en dra nie by tot die hittekapasiteit nie.
As gasmolekules uit meer as twee atome bestaan, sal hulle 6 grade van vryheid hê. Die adiabatiese eksponent in hierdie geval sal gelyk wees aan:
γ=4/3 ≈ 1, 33.
SoDus, soos die aantal atome in 'n gasmolekule toeneem, neem die waarde van γ af. As jy 'n adiabatiese grafiek in die P-V-asse bou, sal jy agterkom dat die kurwe vir 'n monatomiese gas skerper sal optree as vir 'n poliatomiese een.
Adiabatiese eksponent vir 'n mengsel van gasse
Ons het hierbo gewys dat die waarde van γ nie afhang van die chemiese samestelling van die gasstelsel nie. Dit hang egter af van die aantal atome waaruit sy molekules bestaan. Kom ons neem aan dat die stelsel uit N komponente bestaan. Die atoomfraksie van komponent i in die mengsel is 'ni. Dan, om die adiabatiese eksponent van die mengsel te bepaal, kan jy die volgende uitdrukking gebruik:
γ=∑i=1N(aiγ i).
Waar γi die γ-waarde vir die i-de komponent is.
Byvoorbeeld, hierdie uitdrukking kan gebruik word om die γ van lug te bepaal. Aangesien dit uit 99% diatomiese molekules van suurstof en stikstof bestaan, behoort sy adiabatiese indeks baie naby aan die waarde van 1,4 te wees, wat bevestig word deur die eksperimentele bepaling van hierdie waarde.






