Gasse, vanuit die oogpunt van termodinamika, word beskryf deur 'n stel makroskopiese kenmerke, waarvan die belangrikste temperatuur, druk en volume is. Die konstantheid van een van hierdie parameters en die verandering in die ander twee dui aan dat een of ander isoproses in die gas voorkom. Ons sal hierdie artikel wy aan 'n gedetailleerde antwoord op die vrae dat dit 'n isochoriese proses is, hoe dit verskil van isotermiese en isobariese veranderinge in die toestande van 'n gasstelsel.
Ideale gas in fisika

Voordat jy die vraag beantwoord dat dit 'n isochoriese proses is, moet jy die konsep van 'n ideale gas beter leer ken. In fisika word dit verstaan as enige gas waarin die gemiddelde kinetiese energie van sy samestellende deeltjies die potensiële energie van hul interaksie ver oorskry, en die afstande tussen hierdie deeltjies is verskeie grootteordes groter as hul lineêre afmetings. Onder die genoemde toestande is dit moontlik wanneer dit uitgevoer wordberekeninge neem nie die interaksie-energie tussen deeltjies in ag nie (dit is gelyk aan nul), en dit kan ook aanvaar word dat die deeltjies materiaalpunte is met 'n sekere massa m.
Die enigste proses wat in 'n ideale gas plaasvind, is die botsing van deeltjies met die wande van die houer wat die stof bevat. Hierdie botsings manifesteer hulself in die praktyk as die bestaan van 'n sekere druk in die gas P.
As 'n reël kan enige gasvormige stof wat uit relatief chemies inerte molekules bestaan en wat lae druk en hoë temperature het, as 'n ideale gas met voldoende akkuraatheid vir praktiese berekeninge beskou word.
Vergelyking wat 'n ideale gas beskryf
Natuurlik praat ons van die universele wet van Clapeyron-Mendeleev, wat goed verstaan moet word om te verstaan dat dit 'n isochoriese proses is. Dus, die universele toestandsvergelyking het die volgende vorm:
PV=nRT.
Dit wil sê, die produk van die druk P en die gasvolume V is gelyk aan die produk van die absolute temperatuur T en die hoeveelheid stof in mol n, waar R die proporsionaliteitsfaktor is. Die vergelyking self is die eerste keer in 1834 deur Emile Clapeyron neergeskryf, en in die 70's van die 19de eeu het D. Mendeleev 'n stel konstante waardes van 'n enkele universele gaskonstante R (8.314 J/(molK) daarin vervang)).
In ooreenstemming met die Clapeyron-Mendeleev-vergelyking, in 'n geslote stelsel bly die aantal gasdeeltjies konstant, dus is daar net drie makroskopiese parameters wat kan verander (T, Pen V). Laasgenoemde feit lê ten grondslag aan die begrip van die verskillende isoprosesse wat hieronder bespreek sal word.
Wat is 'n isochoriese proses?
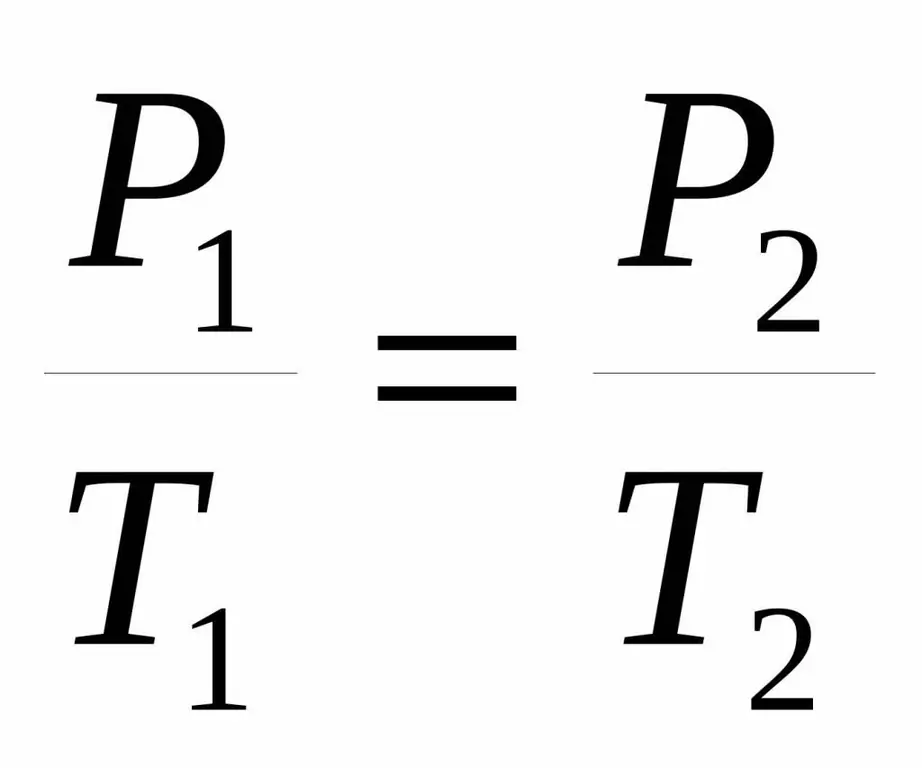
Hierdie proses word verstaan as absoluut enige verandering in die toestand van die stelsel, waarin die volume daarvan behoue bly.
As ons na die universele toestandsvergelyking draai, kan ons sê dat in 'n isochoriese proses slegs druk en absolute temperatuur in 'n gas verander. Om presies te verstaan hoe die termodinamiese parameters verander, skryf ons die ooreenstemmende wiskundige uitdrukking:
P / T=konst.
Soms word hierdie gelykheid in 'n effens ander vorm gegee:
P1 / T1=P2 / T 2.
Albei gelykhede word Charles se wet genoem na die naam van 'n Franse wetenskaplike wat aan die einde van die 18de eeu die bekende afhanklikheid eksperimenteel verkry het.

As ons 'n grafiek bou van die funksie P(T), dan kry ons 'n reguitlyn-afhanklikheid, wat 'n isochoor genoem word. Enige isochoor (vir alle waardes van n en V) is 'n reguit lyn.
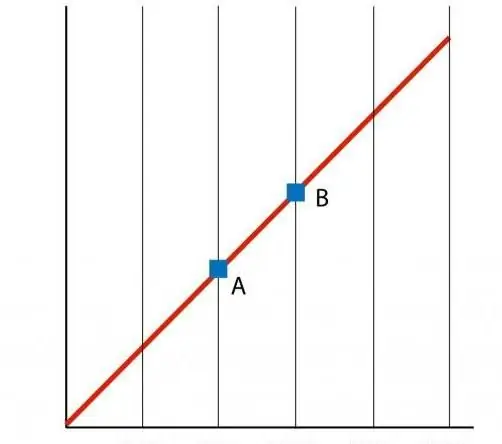
Energiebeskrywing van die proses
Soos opgemerk, is 'n isochoriese proses 'n verandering in die toestand van 'n sisteem wat in 'n geslote maar nie geïsoleerde sisteem plaasvind nie. Ons praat oor die moontlikheid van hitte-uitruiling tussen die gas en die omgewing. Oor die algemeen lei enige toevoer van hitte Q na die stelsel tot twee resultate:
- verander interne energie U;
- gaswerk A, uitbrei of saamtrek.
Die laaste afleiding word wiskundig soos volg geskryf:
Q=U + A.
Die isochoriese proses van 'n ideale gas, volgens sy definisie, impliseer nie werk wat deur die gas gedoen word nie, aangesien die volume daarvan onveranderd bly. Dit beteken dat al die hitte wat aan die stelsel verskaf word, gaan om sy interne energie te verhoog:
Q=U.
As ons die eksplisiete formule vir interne energie in hierdie uitdrukking vervang, dan kan die hitte van die isochoriese proses voorgestel word as:
Q=z / 2nRT.
Hier is z die aantal grade van vryheid, wat bepaal word deur die poliatomiese aard van die molekules waaruit die gas bestaan. Vir 'n monoatomiese gas, z=3, vir 'n diatomiese gas - 5, en vir 'n triatomiese gas - 6. Hier, onder die grade van vryheid, bedoel ons translasie- en rotasiegrade.
As ons die doeltreffendheid van die verhitting van 'n gasstelsel in isochoriese en isobariese prosesse vergelyk, dan sal ons in die eerste geval die maksimum doeltreffendheid kry, aangesien tydens die isobariese verandering in die toestand van die stelsel, die gas uitsit, en 'n deel van die hitte-insette word spandeer om werk te doen.
Isobariese proses
Hierbo het ons in detail beskryf dat dit 'n isochoriese proses is. Kom ons sê nou 'n paar woorde oor ander isoprosesse. Kom ons begin met isobaries. Op grond van die naam word dit verstaan as die oorgang van die sisteem tussen state by konstante druk. Hierdie proses word deur die Gay-Lussac-wet soos volg beskryf:
V / T=konst.
Soos met die isochoor, verteenwoordig die V(T)-isobalk ook 'n reguit lyn op die grafiek.
Virvan enige isobariese proses is dit gerieflik om die werk wat deur die gas verrig word te bereken, aangesien dit gelyk is aan die produk van konstante druk en die verandering in volume.
Isotermiese proses
Dit is 'n proses waarin die temperatuur van die stelsel konstant bly. Dit word beskryf deur die Boyle-Mariotte-wet vir 'n ideale gas. Dit is eienaardig om daarop te let dat dit die eerste eksperimenteel ontdekte gaswet is (tweede helfte van die 17de eeu). Die wiskundige notasie daarvan lyk soos volg:
PV=konst.
Isochoriese en isotermiese prosesse verskil in terme van hul grafiese voorstelling, aangesien die funksie P(V) 'n hiperboliese, nie 'n lineêre verwantskap is nie.
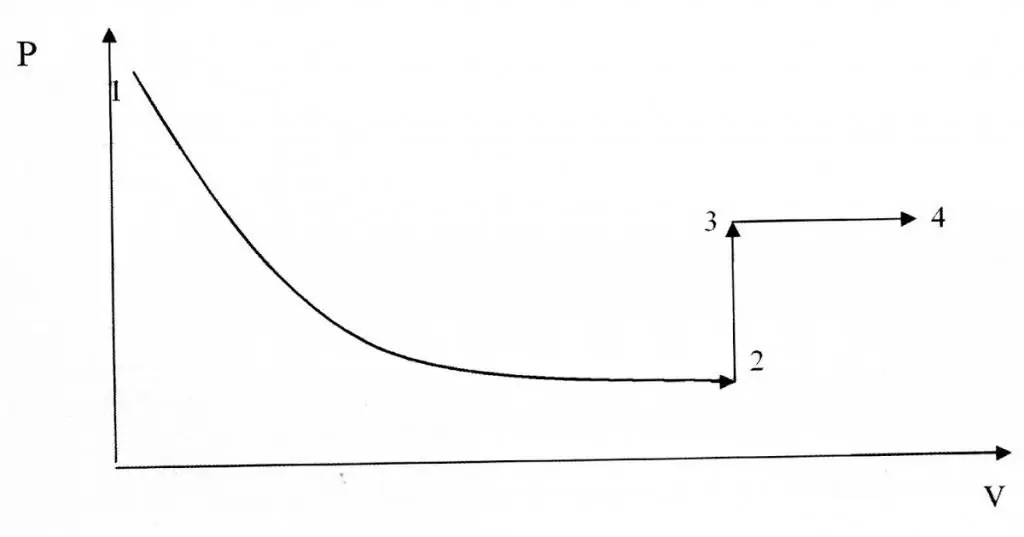
Voorbeeld van probleemoplossing
Kom ons konsolideer die teoretiese inligting wat in die artikel verskaf word deur hul toepassing om 'n praktiese probleem op te los. Dit is bekend dat suiwer gasvormige stikstof in 'n silinder was by 'n druk van 1 atmosfeer en 'n temperatuur van 25 °C. Nadat die gassilinder verhit is en die druk daarin gemeet is, het dit geblyk 1,5 atmosfeer te wees. Wat is die temperatuur van die gas in die silinder na verhitting? Met watter hoeveelheid het die interne energie van die gas verander as daar 4 mol stikstof in die ballon was.
Om die eerste vraag te beantwoord, gebruik ons die volgende uitdrukking:
P1 / T1=P2 / T 2.
Vanwaar ons kom:
T2=P2 / P1 T 1.
In hierdie uitdrukking kan druk in arbitrêre eenhede vervang wordmetings, aangesien hulle krimp, en die temperatuur slegs in kelvin is. Met dit gesê, kry ons:
T2=1.5 /1298.15=447.224 K.
Die berekende temperatuur in grade Celsius is 174 °C.
Aangesien die stikstofmolekule diatomies is, kan die verandering in sy interne energie tydens verhitting soos volg bepaal word:
ΔU=5 / 2nRΔT.
Deur die bekende waardes in hierdie uitdrukking te vervang, kry ons die antwoord op die tweede vraag van die probleem: ΔU=+12.4 kJ.






